A Anvisa (Agência Nacional de Vigilância Sanitária) informou na noite desta segunda-feira (9) que determinou a interrupção do estudo clínico da vacina chinesa Coronavac após a ocorrência de evento adverso grave.
Esse evento, ocorrido no dia 29 de outubro, foi comunicado à agência, que decidiu pausar o estudo para avaliar os dados e julgar sobre o risco/benefício da continuidade do estudo. Com a interrupção, nenhum novo voluntário poderá ser vacinado.
Segundo a Anvisa, os eventos adversos graves são óbitos, incapacidade/invalidez persistente ou significativa, exigência de internação hospitalar do paciente ou prolonga internação, anomalia congênita ou defeito de nascimento e qualquer suspeita de transmissão de agente infeccioso por meio de um dispositivo médico. A agência afirmou que não vai divulgar qual exatamente seria esse ‘evento adverso grave’ ou a localização da ocorrência.
A Coronavac, que é produzida pela chinesa Sinovac e será desenvolvida no Brasil pelo Instituto Butantan, em São Paulo, é a aposta do governador João Doria (PSDB) para controlar a pandemia e virou alvo de críticas por parte do presidente Jair Bolsonaro (sem partido), seu rival político.
Procurada, a Secretaria da Saúde de São Paulo ainda não se manifestou sobre o assunto. Já o Instituto Butantan, esclareceu que foi surpreendido com a decisão da Anvisa e que está apurando em detalhes o que houve com o andamento dos estudos clínicos da Coronavac. O Butantan informou ainda que está à disposição da agência regulatória brasileira para prestar todos os esclarecimentos necessários referentes a qualquer evento adverso que os estudos clínicos podem ter apresentado até o momento.
Em entrevista à Globo News, o professor Dimas Covas, diretor do instituto, disse que a Anvisa foi notificada de um óbito, que não estaria relacionado à vacina. Segundo o diretor, como são mais de 10 mil voluntários dos estudos clínicos em todo o país ao longo de vários meses, é possível que ocorra um acidente ou um problema de saúde que leve ao óbito – sem que necessariamente esteja relacionado à vacina.
Nesta terça (10), às 11h, haverá uma entrevista coletiva à imprensa na sede do instituto.
Regras em estudos clínicos
Segundo a nota divulgada pela Anvisa, esse tipo de interrupção é prevista pelas normativas da Anvisa e faz parte dos procedimentos de Boas Práticas Clínicas esperadas para estudos clínicos conduzidos no Brasil.
“A Anvisa reitera que, segundo regulamentos nacionais e internacionais de Boas Práticas Clínicas, os dados sobre voluntários de pesquisas clínicas devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes”, afirma. “A Anvisa mantém o compromisso com o Estado brasileiro de atuar em prol dos interesses da saúde pública.”
Outros estudos de vacinas contra a Covid-19 interrompidos incluem o da Universidade de Oxford (Reino Unido) com a AstraZeneca e o da empresa Janssen-Cilag (divisão farmacêutica da Johnson & Johnson). Ambos foram retomados após análises.
Na tarde desta segunda (9), Doria afirmou em entrevista a jornalistas que o lote com as primeiras 120 mil doses da Coronavac chega ao país em 20 de novembro. A aplicação, porém, só poderá ser iniciada após a conclusão da fase 3 de testes e a autorização da Anvisa.
Segundo Doria, a agência de vigilância sanitária da China confirmou a liberação da exportação das doses para o Brasil. A importação de seis milhões de vacinas foi autorizada pela Anvisa em 23 de outubro. O total de lotes deve chegar ao país até 30 de dezembro, de acordo com o governador.
As doses que chegarem da China ficarão estocadas no estado de São Paulo. Segundo Dimas Covas, diretor do Instituto Butantan, o local terá segurança reforçada dada a importância do produto.
Covas informou também que tomou conhecimento nesta segunda, ainda em um comunicado extra-oficial, que as autoridades sanitárias chinesas já liberaram a exportação da primeira parte de matéria-prima para a produção da Coronavac pelo Butantan.
O acordo com o governo estadual de São Paulo prevê 46 milhões de doses vindas da China. O Butantan tem capacidade para produzir mais 60 milhões de doses até maio de 2021.
Confira a íntegra da nota da Anvisa:
Após ocorrência de Evento Adverso Grave* a Anvisa determinou a interrupção do estudo clínico da vacina Coronavac. O evento ocorrido no dia 29/10 foi comunicado à Anvisa, que decidiu interromper o estudo para avaliar os dados observados até o momento e julgar sobre o risco/benefício da continuidade do estudo.
Esse tipo de interrupção é prevista pelas normativas da Anvisa e faz parte dos procedimentos de Boas Práticas Clínicas e esperada para estudos clínicos conduzidos no Brasil.
Com a interrupção do estudo, nenhum novo voluntário poderá ser vacinado. A Anvisa reitera que, segundo regulamentos nacionais e internacionais de Boas Práticas Clínicas, os dados sobre voluntários de pesquisas clínicas devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes.
A Anvisa mantém o compromisso com o Estado brasileiro de atuar em prol dos interesses da saúde pública.
*De acordo com a RDC 09/2015 são considerados eventos adversos graves:
- a) óbito;
- b) evento adverso potencialmente fatal (aquele que, na opinião do notificante, coloca o indivíduo sob risco imediato de morte devido ao evento adverso ocorrido);
- c) incapacidade/invalidez persistente ou significativa;
- d) exige internação hospitalar do paciente ou prolonga internação;
- e) anomalia congênita ou defeito de nascimento;
- f) qualquer suspeita de transmissão de agente infeccioso por meio de um dispositivo médico;
- g) evento clinicamente significante.
Categoria
Saúde e Vigilância Sanitária

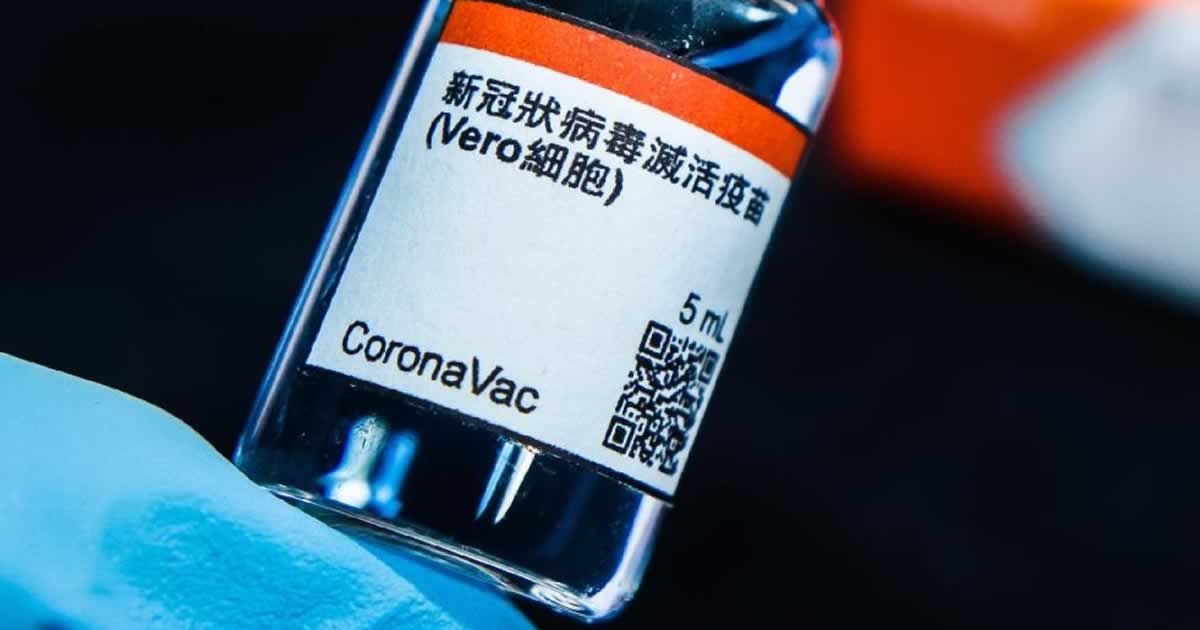


O “evento adverso” não tem qualquer relação com o teste da Vacina: tratou-se, infelizmente, de suicídio.
Logo, o site deveria replicar a informação nova.